高张力环炔介导的羰基1,2-转位新策略。 2026年4月17日,华南理工大学吴钊课题组在Nature Synthesis期刊上发表了题为 Angle-strained cycloalkyne-mediated carbonyl 1,2-transposition的研究论文。该研究首次提出并实现了基于高张力环炔中间体的羰基1,2-转位新策略,成功解决了环戊酮等小环酮类化合物骨架编辑长期存在的合成难题,为药物分子后期修饰与复杂天然产物的快速衍生化提供了高效、普适的新工具。
该论文的第一作者为华南理工大学前沿软物质学院博士研究生季侃磊,通讯作者为吴钊教授,华南理工大学为唯一通讯单位。
羰基1,2-转位是指将酮羰基从一个碳原子迁移到相邻碳原子上的反应。这一看似简单的转化,能够显著改变分子的几何形状、电子分布和生物活性,在新药研发和天然产物全合成中具有重要应用价值。然而,现有方法多依赖贵金属催化或底物特异性的链行走异构化体系,不仅操作繁琐、试剂昂贵,而且对环戊酮等小环酮类底物束手无策。特别是环戊酮的羰基迁移,自该领域诞生以来始终未能实现通用性解决方案。针对上述挑战,研究团队独辟蹊径地提出了高张力环炔介导的羰基迁移新策略。其核心思想是:利用小环炔(环戊炔、环己炔)因角度变形而蕴含的巨大环张力(环戊炔的理论张力能高达81 kcal/mol),将其作为驱动骨架重排的内置发动机。具体过程为:从商品化的环酮出发,在温和条件下原位生成烯基三氟甲磺酸酯,随后经碱诱导消除产生高张力环炔中间体。这一高活性中间体会被反应体系中的双(三甲基硅基)氨基钠(NaHMDS)以极高的区域选择性捕获,形成烯胺,最后经水解即可一步得到羰基迁移产物。整个操作仅需常用试剂和一锅法反应,无需分离任何中间体(图1)。
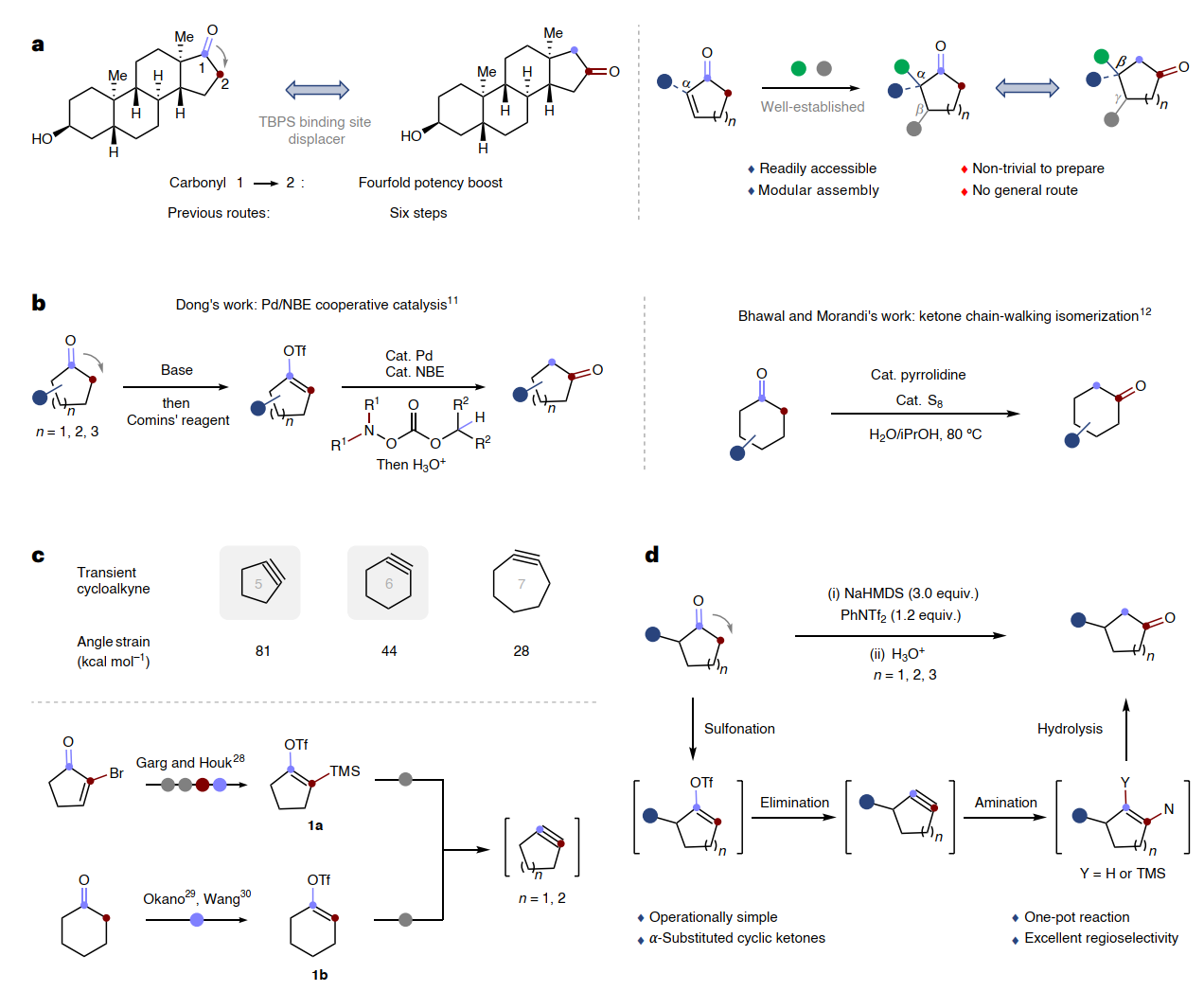
图1:羰基1,2-转位反应与高张力环炔策略。
该方法展现出极其广泛的底物适用性。无论是环戊酮还是环己酮,无论是α-单取代、α,α-双取代、螺环还是桥环结构,均能以良好至优异的产率获得目标迁移产物。特别值得一提的是,研究团队成功将该方法应用于多种结构复杂的天然产物和药物分子的后期骨架编辑,包括:诺品酮、薄荷酮等萜类;脱氢表雄酮(DHEA)、表雄酮、雌酚酮甲醚等甾体;毛瑞素(mutilin)衍生物与齐墩果酸甲酯等。这些复杂分子的高效转化充分展示了该方法在药物化学和天然产物合成中的巨大应用潜力(图2)。

图2:底物范围。
除了直接的羰基迁移,研究团队还发展了一系列串联环化-迁移策略,将经典的环丙烷化、[2+2]环加成、Diels-Alder反应与羰基迁移相融合,实现了传统多步合成难以企及的β,γ-双官能化稠环骨架的一步构建。例如,从简单原料出发,仅需两步即可获得含有相邻季碳中心的顺式-3,5-稠环结构,而传统方法通常需要五步以上且总产率极低(图3)。

图3:合成应用。
研究团队通过环加成捕获实验与烯胺中间体原位表征实验,为环炔中间体介导的羰基迁移提供了证据,阐明了区域选择性的电子/位阻控制模型,为后续利用其他高张力中间体发展新型分子编辑反应奠定了理论基础。
研究得到了国家自然科学基金、广东省基础与应用基础研究基金、广东省珠江人才团队、广州市科技计划与TCL 科技创新基金等项目的资助。(来源:科学网)
相关论文信息:https://doi.org/10.1038/s44160-026-01059-8
作者:吴钊 等 来源:《自然-合成》

